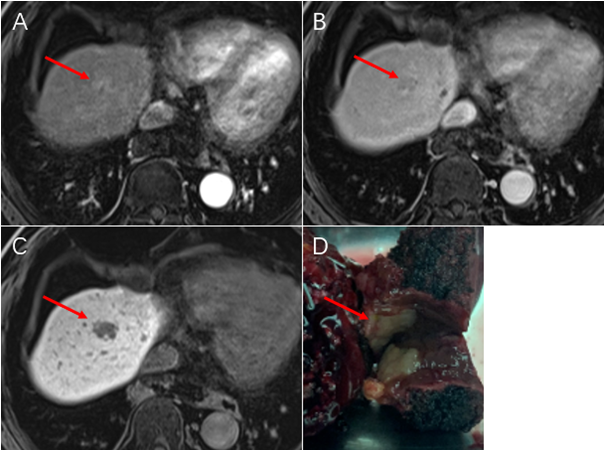
图1 ICC的治疗策略¹

图2. ICC、pCC和dCC的解剖位置¹
单纯评估可切除ICC辅助治疗的研究较为少见,研究通常会同时纳入胆囊癌和其他胆道肿瘤患者。PRODIGE 12-ACCORD 18研究是一项多中心、开放标签、随机、III期临床试验,研究共纳入196例接受了R0或R1切除术的胆道恶性肿瘤患者,患者被随机分配接受吉西他滨+奥沙利铂(GEMOX)化疗或仅行观察。在中位随访46.5个月时,研究表明化疗患者的无复发生存期(RFS)未显示统计学上的获益(HR=0.88;95%CI,0.62-1.25;p=0.48),OS同样未显示获益(HR=1.08;95%CI,0.70-1.66;p=0.74)?。
对于可切除的ICC患者,新辅助治疗存在多种理论上的获益,包括抑制微转移灶以降低疾病的早期复发风险、缩瘤降期以实现R0切除等,然而目前ICC患者的新辅助治疗获益情况尚未得到前瞻性大型III期随机对照研究的证实。
另有三项临床研究正在进行中,其中一项单中心II期试验NCT03603834旨在评估mFOLFOXIRI(5-FU+LV+伊立替康+奥沙利铂)在交界可切除胆管癌(ICC/pCC/dCC)新辅助治疗的疗效;多中心、随机对照、开放标签、III期GAIN试验旨在评估吉西他滨+顺铂围手术期化疗在可切除和交界可切除胆管癌(ICC/pCC/dCC)患中的疗效和安全性;OPT-IC研究则评估了吉西他滨+顺铂+白蛋白紫杉醇在ICC患者新辅助治疗中的应用,值得注意的是,该研究同时探索了FGFR2抑制剂在FGFR2融合性ICC患者新辅助治疗的应用。
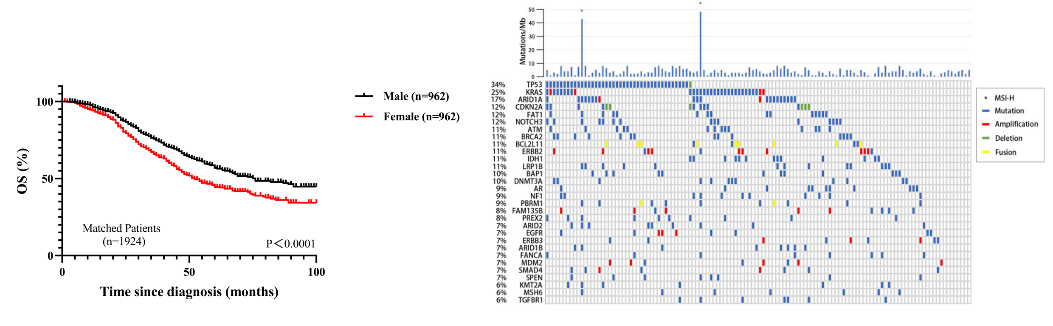
IDH1突变约见于25%的ICC患者²²,既往一项纳入73例IDH1突变型胆管癌患者的I期研究显示,IDH1抑制剂艾伏尼布应用后患者中位PFS为3.8个月,中位OS为13.8个月²²。基于这一疗效,III期随机对照ClarIDHy试验评估了艾伏尼布对比安慰剂在IDH突变型胆管癌患者中的应用,结果显示,艾伏尼布组患者的中位PFS存在显著改善(2.7个月 vs. 1.4个月;HR=0.37;95%CI,0.24-0.54;p<0.0001),中位OS存在数值上的改善,但无统计学意义(10.3个月 vs. 7.5个月;HR=0.79;95%CI,0.56-1.12;p=0.09)。特别地,该研究存在57%的患者交叉现象,在基于交叉进行调整后,安慰剂组的中位OS为5.1个月(HR=0.49;95%CI,0.34-0.70;p<0.001)²³,²?。
ICC是一种罕见但侵袭性较强且预后较差的恶性肿瘤,其发病率正在增加。手术切除和细胞毒性治疗分别是早期ICC和晚期或转移性ICC的重要治疗手段,以此为基础的多学科治疗正显著改善ICC患者的预后情况。本文对ICC患者的药物治疗策略进行了回顾:对于局限性和可切除ICC患者,根治性手术联合术后卡培他滨辅助治疗应成为标准治疗;对于不可切除或转移性ICC患者,局部治疗、三联全身治疗、靶向治疗和免疫治疗正得到越来越多的认可,已为经过筛选的患者群体带来了令人欣喜的疗效。多项与上述疗法相关的临床研究正在进行中,期待未来这些研究结果的公布可以为ICC患者带来更多治疗获益。
参考文献(向上滑动查看):
1. Moris D, Palta M, Kim C, et al. Advances in the treatment of intrahepatic cholangiocarcinoma: An overview of the current and future therapeutic landscape for clinicians. CA Cancer J Clin. 2023 Mar;73(2):198-222.
2. Moris D, Palta M, Kim C, et al. Advances in the treatment of intrahepatic cholangiocarcinoma: An overview of the current and future therapeutic landscape for clinicians[J]. CA: A Cancer Journal for Clinicians, 2022.
3. Blechacz B, Komuta M, Roskams T, et al. Clinical diagnosis and staging of cholangiocarcinoma[J]. Nature reviews Gastroenterology & hepatology, 2011, 8(9): 512-522.
4. Rizvi S, Gores G J. Pathogenesis, diagnosis, and management of cholangiocarcinoma[J]. Gastroenterology, 2013, 145(6): 1215-1229.
5. Saha S K, Zhu A X, Fuchs C S, et al. Forty-year trends in cholangiocarcinoma incidence in the US: intrahepatic disease on the rise[J]. The oncologist, 2016, 21(5): 594-599.
6. Edeline J, Benabdelghani M, Bertaut A, et al. Gemcitabine and oxaliplatin chemotherapy or surveillance in resected biliary tract cancer (PRODIGE 12-ACCORD 18-UNICANCER GI): a randomized phase III study[J]. Journal of Clinical Oncology, 2019, 37(8): 658-667.
7. Primrose J N, Fox R P, Palmer D H, et al. Capecitabine compared with observation in resected biliary tract cancer (BILCAP): a randomised, controlled, multicentre, phase 3 study[J]. The Lancet Oncology, 2019, 20(5): 663-673.
8. Yadav S, Xie H, Bin-Riaz I, et al. Neoadjuvant vs. adjuvant chemotherapy for cholangiocarcinoma: a propensity score matched analysis[J]. European Journal of Surgical Oncology, 2019, 45(8): 1432-1438.
9. Mason M C, Massarweh N N, Tzeng C W D, et al. Time to REThink upfront surgery for resectable intrahepatic cholangiocarcinoma? Implications from the neoadjuvant experience[J]. Annals of surgical oncology, 2021, 28(11): 6725-6735.
10. Maithel, Shishir K., et al. "NEO-GAP: A phase II single-arm prospective feasibility study of neoadjuvant gemcitabine/cisplatin/nab-paclitaxel for resectable high-risk intrahepatic cholangiocarcinoma." (2022): 4097-4097.
11. Martin, Robert CG, et al. "Drug-Eluting Bead, Irinotecan Therapy of Unresectable Intrahepatic Cholangiocarcinoma (DELTIC) with Concomitant Systemic Gemcitabine and Cisplatin." Annals of Surgical Oncology (2022): 1-12.
12. Ensminger, W. D., and J. W. Gyves. "Clinical pharmacology of hepatic arterial chemotherapy." Seminars in oncology. Vol. 10. No. 2. 1983.
13. Jarnagin, W. R., et al. "Regional chemotherapy for unresectable primary liver cancer: results of a phase II clinical trial and assessment of DCE-MRI as a biomarker of survival." Annals of oncology 20.9 (2009): 1589-1595.
14. Kemeny, Nancy E., et al. "Treating primary liver cancer with hepatic arterial infusion of floxuridine and dexamethasone: does the addition of systemic Bevacizumab improve results." Oncology 80.3-4 (2011): 153-159.
15. Cercek, Andrea, et al. "Assessment of hepatic arterial infusion of floxuridine in combination with systemic gemcitabine and oxaliplatin in patients with unresectable intrahepatic cholangiocarcinoma: a phase 2 clinical trial." JAMA oncology 6.1 (2020): 60-67.
16. Valle, Juan, et al. "Cisplatin plus gemcitabine versus gemcitabine for biliary tract cancer." New England Journal of Medicine 362.14 (2010): 1273-1281.
17. Morizane, C., et al. "Combination gemcitabine plus S-1 versus gemcitabine plus cisplatin for advanced/recurrent biliary tract cancer: the FUGA-BT (JCOG1113) randomized phase III clinical trial." Annals of Oncology 30.12 (2019): 1950-1958.
18. Desrame, Jérôme, et al. "Modified FOLFIRINOX versus CISGEM chemotherapy for patients with advanced biliary tract cancer (PRODIGE 38 AMEBICA): A randomized phase II study." Journal of Clinical Oncology 40.3 (2022): 262-271.
19. Shroff, Rachna T., et al. "Gemcitabine, cisplatin, and nab-paclitaxel for the treatment of advanced biliary tract cancers: a phase 2 clinical trial." JAMA oncology 5.6 (2019): 824-830.
20. Abou-Alfa, Ghassan K., et al. "pemigatinib for previously treated, locally advanced or metastatic cholangiocarcinoma: a multicentre, open-label, phase 2 study." The Lancet Oncology 21.5 (2020): 671-684.
21. Javle, Milind, et al. "Phase II study of BGJ398 in patients with FGFR-altered advanced cholangiocarcinoma." Journal of Clinical Oncology 36.3 (2018): 276.
22. Lowery, Maeve A., et al. "Safety and activity of ivosidenib in patients with IDH1-mutant advanced cholangiocarcinoma: a phase 1 study." The lancet Gastroenterology & hepatology 4.9 (2019): 711-720.
23. Abou-Alfa, Ghassan K., et al. "Ivosidenib in IDH1-mutant, chemotherapy-refractory cholangiocarcinoma (ClarIDHy): a multicentre, randomised, double-blind, placebo-controlled, phase 3 study." The Lancet Oncology 21.6 (2020): 796-807.
24. Zhu, Andrew X., et al. "Final overall survival efficacy results of ivosidenib for patients with advanced cholangiocarcinoma with IDH1 mutation: the phase 3 randomized clinical ClarIDHy trial." JAMA oncology 7.11 (2021): 1669-1677.
25. Oh DY, et al. durvalumab plus Gemcitabine and Cisplatin in Advanced Biliary Tract Cancer. NEJM Evid. 2022 Aug;1(8):EVIDoa2200015.
26. Vogel, Arndt, et al. "Regional subgroup analysis of the phase 3 TOPAZ-1 study of durvalumab (D) plus gemcitabine and cisplatin (GC) in advanced biliary tract cancer (BTC)." 2022 ASCO Abstract 4075.
27. Richard S. Finn, et al. pembrolizumab (pembro) plus gemcitabine and cisplatin (gem/cis) compared with gem/cis alone for patients (pts) with advanced biliary tract cancer (BTC): Updated efficacy and safety from KEYNOTE-966. 2023 ESMO ASIA Congress. 133MO.